Research
私たちは、機能性生体分子を創製し、細胞機能や遺伝子を精密にコントロールすることを目指しています。生命現象の深層的な理解を追求するとともに、その成果を革新的な創薬や細胞機能制御技術の開発へと繋げ、未来の生命科学・医療に貢献していきます。
1.DNAやRNAに結合する人工タンパク質で遺伝子を操る、知る
DNAシーケンシング技術やゲノム編集技術の発展によって、現在では、ゲノムの配列情報が簡単に得られ、またゲノム配列を操作できるようになりました。しかし、核酸にはまだ未知の機能がたくさんひそんでいると考え、塩基配列情報にとどまらない核酸の機能の解明に取り組んでいます。特に、生命活動をリアルタイムで調節する上で中心的な役割を果たすRNAに着目し、核酸の化学修飾や高次構造といった高次情報を検出し、精密に調節、利用する方法論を確立することで、遺伝子の多元性にせまるとともに、疾患に対するこれまでにない診断・治療法につなげたいと考えています。
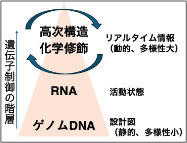
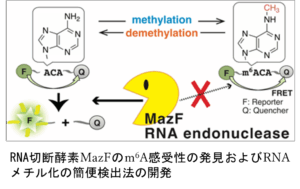
1.1. RNAの化学修飾を調節するタンパク質の機能デザイン、作用機序解明
A, C, G, Uといった塩基のほかに、RNAには170種類以上もの化学修飾があることが知られています。しかし、これらの修飾が生命システムの中でどのような機能を持つのかの全貌は明らかになっていません。
私たちは、mRNAに多く見られるメチル化アデノシン(m6A)に着目し、まず、m6Aを簡単に検出する方法を開発しました。さらにこの方法を用いて、m6Aに作用する脱メチル化酵素の阻害剤を見出しました。また、狙った配列にピンポイントで、かつ刺激に応答してRNAのメチル化状態を操作できるようなタンパク質の機能デザインに成功しています。より高選択性、高効率化に向けたタンパク質デザインと、細胞内での応用に向けて研究を進めています。
Chem. Commun., 2017, 2020, 2023, 2025

1.2. RNAの高次構造の多彩な機能の解明、高次構造を介した遺伝子制御
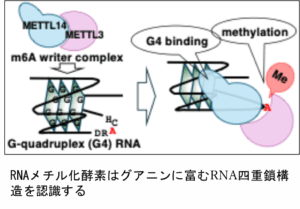
RNAは一本鎖、二重らせん構造をはじめとして、ヘアピン構造など多様な構造を形成します。中でも最近注目されているのは、グアニンに富む配列中で形成されるグアニン四重らせん構造(G-quadruplex: G4)と呼ばれる非標準な構造です。G4はがんや神経変性疾患にも関わることが示唆されていますが、細胞の中で、どのRNA中でG4構造が形成されているのかということをはじめとして、その実態はほとんどわかっていません。
私たちは、アデノシンのメチル化をつかさどる酵素がRNAのG4構造に結合しやすく、その近傍をメチル化しやすいことを見出しました。この知見は、RNAの高次構造がRNAの化学修飾の調節に関係している可能性を示唆しており、塩基の並びだけからは読み取れないRNAの多彩な機能の一例であると考えられます。現在、G4構造を特異的に認識する機能を持ったペプチドのデザインや、細胞の中でのG4構造の化学的な検出法の開発に取り組んでいます。
NAR 2022, ChemBioChem2025など
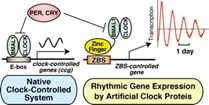
1.3. 人工転写因子による体内時計の制御
私たちは、ジンクフィンガー型転写因子の特徴であるDNA 認識様式の設計の柔軟性・多様性を利用して、人工的なDNA結合タンパク質を創製してきました。そして、人為的に作製した転写因子タンパク質を用いて細胞内の概日リズムを調節することに世界で初めて成功しました(京都大学薬学研究科岡村教授との共同研究)。また、概日リズムを人工的に産み出し、制御する新しい転写制御系を創出することにより、概日リズムが細胞レベルでどのような影響を与えるかを調べる試みも行ってきました。
Angew. Chem. Int. Ed. 2011, ACS Chem. Biol. 2012など
2.機能性分子の細胞内送達と細胞機能の制御
近年、データベース科学やニューラルネットワーク、遺伝子組換え技術の構築に加え、機械学習の進歩により、疾患原因遺伝子や分子異常が迅速に見出されるようになってきました。しかし、それらの多くは天然変性タンパク質やその凝集体、タンパク質間相互作用など、従来の低分子医薬品では制御が難しい undruggable な標的であることが大きな課題となっています。
これらの高難度疾患標的の制御に向けて、抗体医薬、核酸医薬、遺伝子治療など多様な創薬モダリティの開発が進められています。抗体医薬は優れた抗原特異性を有する一方で、膜透過性に欠けることから、その標的は主に細胞外分子に限定されています。また、核酸医薬においても mRNA ワクチンなどの成功例がある一方、細胞膜透過性を持たないため、脂質ナノ粒子をはじめとする細胞内導入キャリアが不可欠です。
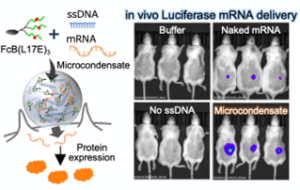
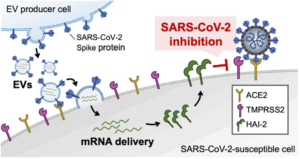
これに対して私たちの研究室では、抗体や核酸を含む高分子医薬を細胞内へ効率的かつ安全に送達するための薬物送達キャリアの開発に取り組んでいます。具体的には、ペプチドや機能性タンパク質を基盤とした分子設計に加え、コアセルベートや細胞外小胞(Extracellular Vesicles, EVs)といった分子集合体・生体由来キャリアを活用することで、多様な分子を細胞内へ導入する技術の創出を進めています。
これらの送達技術を通じて、天然変性タンパク質やタンパク質間相互作用といった undruggable な標的を制御し、細胞機能の理解と人為的操作を可能にすることで、次世代の創薬研究や新規創薬モダリティの確立へとつなげることを目指しています。